オメガ3系不飽和脂肪酸とオメガ6系不飽和脂肪酸
【ω3 系とω6 系の不飽和脂肪酸はその働きに大きな違いがある】
脂肪酸には、飽和脂肪酸と不飽和脂肪酸があり、飽和脂肪酸では、炭化水素鎖の全ての炭素が水素で飽和しています。一方、不飽和脂肪酸では炭化水素鎖中に1個ないし数個の二重結合(CH=CH)が含まれます。不飽和脂肪酸中で二重結合の数が2個以上のものを多価不飽和脂肪酸と云い、5 個以上の二重結合を持つ脂肪酸を高度不飽和脂肪酸と呼びます。
多価不飽和脂肪酸にはオメガ3系とオメガ6系があります。
脂肪酸の種類
主な脂肪酸名
主な性質
多く含む食用油
飽和脂肪酸パルミチン酸
ステアリン酸肉、卵、乳製品など動物性食品に多く含まれる。コレステロールが多く固まりやすい。
マーガリン、ラード、バター、牛脂
一価不飽和
脂肪酸オメガ9
(n-9)オレイン酸
オリーブやアボカド、ナッツ類に多く含まれる、酸化されにくい。
オリーブ油、菜種油、米油、落花生油、
多価不飽和
脂肪酸オメガ6
(n-6)リノール酸
γ-リノレン酸
アラキドン酸大豆やゴマやトウモロコシ等食材に多く含まれる。リノール酸は体内で生成できない必須脂肪酸
大豆油、コーン油、ゴマ油、グレープシードオイル
オメガ3
(n-3)α-リノレン酸
エイコサペンタエン酸
ドコサヘキサエン酸魚類、亜麻仁、エゴマ、クルミなどに多く含まれる。α-リノレン酸は体内で生成できない必須脂肪酸。酸化されやすい。
魚油、亜麻仁油、紫蘇油(エゴマ油)、クルミ油
表:主な長鎖脂肪酸の種類と特徴。脂肪酸は飽和脂肪酸と不飽和脂肪酸に分けられ、多価不飽和脂肪酸にはオメガ3系とオメガ6系がある。がんの予防や治療には、ω9系の一価不飽和脂肪酸のオレイン酸とω3系多価不飽和脂肪酸のα-リノレン酸、エイコサペンタエン酸、ドコサヘキサエン酸を多く摂取し、飽和脂肪酸とω6系多価不飽和脂肪酸は減らすことが望ましい。
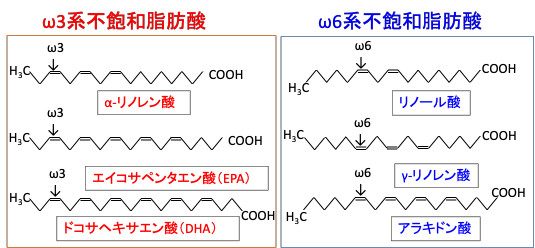
リノール酸 CH3(CH2)3 CH2CH=CHCH2CH=CH(CH2)7COOH では、CH3 に最も近い二重結合は、CH3から6番目のCにあります。この位置に二重結合を持つ全ての脂肪酸をω6系不飽和脂肪酸に分類します。
α-リノレン酸CH3CH2CH=CHCH2CH=CHCH2CH=CH(CH2)7COOH では、CH3に最も近い二重結合はCH3から3番目のC にあります。この位置に二重結合を持つ全ての脂肪酸をω3系不飽和脂肪酸に分類します。
最近ではω6の代わりにn-6 を用いてn-6系不飽和脂肪酸、そしてω3の代わりにn-3を用いてn-3系不飽和脂肪酸と呼ぶことが多くなっています(図)。
図:ω3系不飽和脂肪酸とω6系不飽和脂肪酸の化学構造。構造式では連結部の炭素(C)と炭素と結合する水素(H)は省略されている。メチル基(CH3)側から数えた炭素の番号はω1(あるいはn-1)、ω2(あるいはn-2)と表示する。最初の二重結合がω3の位置にある不飽和脂肪酸をω3系不飽和脂肪酸あるいはn-3系不飽和脂肪酸と言い、ω6の位置にある不飽和脂肪酸をω6系不飽和脂肪酸あるいはn-3系不飽和脂肪酸と呼ぶ。
ω6 系不飽和脂肪酸はリノール酸 → γ-リノレン酸 → アラキドン酸のように代謝されていき、アラキドン酸からプロスタグランジン、ロイコトリエン、トロンボキサンなどの重要な生理活性物質が合成されます。プロスタグランジンなどのアラキドン酸代謝産物は炎症や細胞のがん化を促進したり、がん細胞の増殖を速める作用があるのですが、体のいろんな生理作用に必要であるため、動物は食物(植物および肉類)からリノール酸を摂取しなければ生存できません。
ω3系不飽和脂肪酸はα-リノレン酸 → エイコサペンタエン酸(EPA) → ドコサヘキサエン酸(DHA)と代謝されていきます。ただし、人間の体内ではα-リノレン酸からエイコサペンタエン酸(EPA)への変換は極めて少なく、ドコサヘキサエン酸(DHA)への変換はほとんどゼロだと言われています。したがって、α-リノレン酸を多く摂取してもEPAやDHAのような抗がん作用や健康作用は得られません。
ω3 系不飽和脂肪酸は炎症やアレルギーを抑え、血栓の形成や動脈硬化やがん細胞の発育を抑える作用があります。したがって、食物中のα-リノレン酸/リノール酸の比を上げると、血栓性疾患、脳梗塞および心筋梗塞、炎症、アレルギー、発がん、がんの転移、高血圧などの発症率が低下すると考えられています。
EPAやDHAを前駆体として生成されるレゾルビンやプロテクチンという物質が、炎症の収束に重要な役割を果たしていることが明らかになっています。つまり、DHAやEPAを多く摂取すると体内の炎症を抑制し、これががん予防効果の一つのメカニズムになっているようです。
食事から摂取された脂肪は代謝されてエネルギー源となり、また分解されて生成した脂肪酸は細胞膜などに取り込まれます。細胞膜の構成成分として使われる場合、その脂肪酸自体は変化せず、それぞれの構造や性質を保ったまま使われます。
つまり、細胞膜をつくるとき脂肪酸の違いを区別せず、手当たり次第にあるものを使用するのです。その結果、食事中の脂肪酸の種類によって細胞の性質も変わってきます。
さらに、その細胞膜の脂肪酸から作られるプロスタグランジンやロイコトリエンなどの化学伝達物質の種類も違ってきて、炎症やアレルギー反応や発がんに影響することが明らかになっています。
例えば、リノール酸のようなω6系不飽和脂肪酸を多く摂取すると、血栓ができやすくなり、アレルギー反応を増悪させ、がんの発生頻度を高めます。ω6系不飽和脂肪酸を多く取り込んだがん細胞は増殖が早く転移をしやすくなります。
一方、魚油に多く含まれるドコサヘキサエン酸(DHA)やエイコサペンタエン酸(EPA)のようなω3不飽和脂肪酸を多く摂取すると、炎症やアレルギーを抑え、血栓の形成や動脈硬化やがん細胞の発育を抑える作用があります。DHAやEPAを多く摂取するとがん細胞が抗がん剤で死にやすくなることも報告されています。その理由は、食事から摂取されたω3不飽和脂肪酸ががん細胞の膜の脂質組成を変えることによって細胞シグナル系に影響して増殖を抑えるからです。
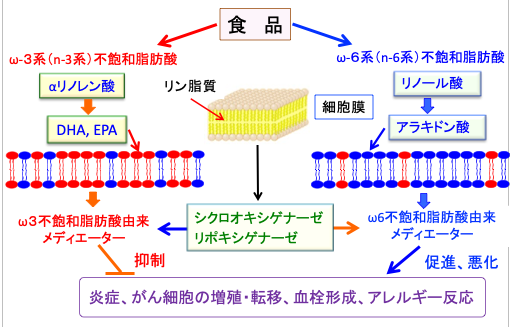
図:食品から摂取される脂肪酸はそのまま細胞膜の脂質二重層に組み込まれる。食事からのリノール酸やアラキドン酸の摂取が多いと細胞膜のアラキドン酸(細胞膜の図の青で示す)の量が増え、ω6不飽和脂肪酸由来のメディエーターの産生量も増える。一方、ω3系不飽和脂肪酸のドコサヘキサエン酸(DHA)やエイコサペンタエン酸(EPA)の摂取量が多いと、DHAやEPA(細胞膜の図の赤で示す)がアラキドン酸と置き換わるので、ω6不飽和脂肪酸由来のメディエーターの産生は低下し、ω3不飽和脂肪酸由来のメディエーターが増える。炎症やがん細胞の増殖・転移、血栓形成、アレルギー反応はω6不飽和脂肪酸由来メディエーターで促進・悪化され、ω3不飽和脂肪酸由来のメディエーターは抑制する。不飽和脂肪酸のω6:ω3の比を低下させると、がん細胞の増殖抑制、抗がん剤や放射線治療による正常組織のダメージの軽減や悪液質の改善の効果が増強する。
人間を含め哺乳動物は体内でオメガ6とオメガ3の不飽和脂肪酸を合成できないので、食事から取り入れています。つまり、体内で自分でつくることができないので、食事の変更による生体機能の変更を行うときの重要なターゲットになります。
食事中の脂肪酸の種類によるがん細胞への影響の違いを知ることは、がんを抑える食事療法の実践において、極めて重要です。
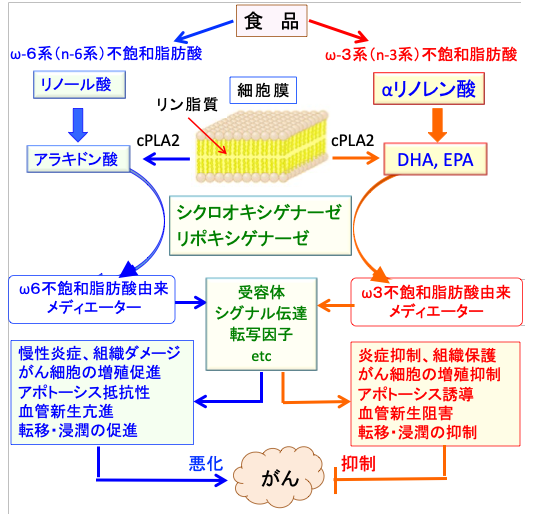
図:ω6系(n-6系)多価不飽和脂肪酸のアラキドンサンはプロスタグランジンE2やロイコトリエンなど炎症性メディエーターを産生して炎症や組織のダメージを悪化させ、がん細胞の増殖を促進する作用を持つ。一方、ω3系(n-3系)多価不飽和脂肪酸であるEPA(エイコサペンタエン酸)とDHA(ドコサヘキサエン酸)は代謝されて抗炎症作用を示す多様な脂質メディエーターを産生することによって、慢性炎症や組織のダメージを軽減する効果や、がん細胞の増殖を抑える効果を発揮する。この抗炎症作用や組織保護作用は抗がん剤や放射線治療による正常組織のダメージの軽減や悪液質の改善にも役立つ。食事から摂取したDHAやEPAは細胞膜に取り込まれ、細胞膜脂質二重層中のアラキドン酸と入れ替わるので、DHAやEPAの摂取が多いと炎症やがんの進行を抑制する効果が得られる。
【DHAとEPAは抗炎症性メディエーターの前駆体】
DHAやEPAには抗炎症作用や鎮痛作用があります。実際に関節炎などの痛みを緩和し、CRPなどの炎症マーカーを低下させる作用もあります。そのメカニズムとしては、プロスタグランジンE2などの炎症を引き起こす物質を生み出すω6系のアラキドン酸がω3系のDHAやEPAに置き換えられ、したがって炎症物質ができにくくなるから、といわれていました。
すなわち、ω3系不飽和脂肪酸を多く摂取すると、細胞膜中のω3系不飽和脂肪酸が増加して、アラキドン酸濃度が低下するので、その結果アラキドン酸由来の炎症促進性物質の産生が抑制されるという機序です。
しかし、最近の研究では、ω3系不飽和脂肪酸のDHAとEPAが炎症を抑える物質を生成することが明らかになっています。
外傷や感染などに反応して急性炎症反応が起こりますが、異物の排除が完了すると炎症反応は速やかに消散し、組織の修復過程に移行します。炎症反応が終了することを「炎症の収束(resolution of inflammation)」と言います。
炎症の収束は、これまで起炎反応の減弱化によると考えられてきましたが、最近の研究で、受動的なものではなく、能動的な機構であることが明らかになっています。
急性炎症の特徴は白血球の組織への浸潤に伴う浮腫、発赤、発熱、痛みなどで、これらの反応にはアラキドン酸から生成されるプロスタグランジンやロイコトリエンなどの脂質メディエーターが関与します。これらの物質によって好中球の浸潤や活性化、血管透過性の亢進などの炎症反応が起こります。
炎症の収束過程においては炎症性サイトカインの産生が抑制され、血管透過性が正常に戻り、好中球の遊走阻止や浸出液中のリンパ球の除去や、マクロファージによる死滅した細胞の除去などが起こります。この炎症の収束過程には、EPAやDHAなどのオメガ3系不飽和脂肪酸から体内で生成されるレゾルビンやプロテクチンという抗炎症性メディエーターが関与します。
つまり、ω3系脂肪酸はアラキドン酸と競合することで炎症性ケミカル・メディエーターの産生を阻害するだけでなく、DHAやEPAは抗炎症性(炎症収束性)の脂質メディエーターを生成することによって積極的に炎症を抑制する作用があるのです。
EPAやDHAの抗炎症作用やがん予防効果や心血管保護作用や脳神経系保護作用など多くの作用に、EPAやDHAから代謝されて生成される抗炎症性の脂質メディエーター(レゾルビンやプロテクチン)が関与しているようです。
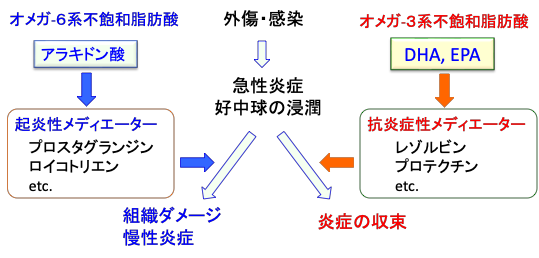
図:オメガ6系不飽和脂肪酸は炎症を促進する化学伝達物質(メディエーター)を産生し、オメガ3系不飽和脂肪酸のドコサヘキサエン酸(DHA)やエイコサペンタエン酸(EPA)は炎症を抑制する化学伝達物質を産生し、炎症を収束させる。
【ω3系不飽和脂肪酸/ω6系不飽和脂肪酸の比を上げるとがん細胞はおとなしくなる】
細胞膜はタンパク質や脂肪酸や糖質から作られます。細胞膜の脂肪酸は食物から摂取された脂肪酸がそのまま取り込まれるため、食事中の脂肪酸の違いによって細胞の性質を変えることができます。その理由は、細胞膜の脂肪酸から作られるプロスタグランジンやロイコトリエンなどの化学伝達物質の種類が違ってくるからです。
リノール酸やγ-リノレン酸やアラキドン酸のようなω6系不飽和脂肪酸を多く取り込んだがん細胞は増殖が早く転移しやすくなります。一方、魚油に多く含まれるドコサヘキサエン酸(DHA)やエイコサペンタエン酸(EPA)やα-リノレン酸のようなω3不飽和脂肪酸を多く取り込んだがん細胞は増殖が抑えられ、抗がん剤で死にやすくなります。
ω6系不飽和脂肪酸は、がん細胞の増殖や血管新生を促進するプロスタグランジンE2の原料になり、ω3系不飽和脂肪酸はプロスタグランジンE2の産生を抑えることが関連しています。
プロスタグランジンE2(PGE2)は細胞の増殖や運動を活発にしたり、細胞死が起こりにくくする生理作用があるため、がん細胞の増殖や転移を促進します。PGE2はω6 系不飽和脂肪酸はリノール酸から合成され、DHAなどのω3 系不飽和脂肪酸はPGE2が体内で増えるのを抑える働きがあります。
DHAががんの予防や治療の効果を高めることは多くの臨床的研究や実験的研究で明らかになっています。毎日魚を食べている人は、そうでない人に比べ大腸がんや乳がんや前立腺がんなど欧米型のがんになりにくいという研究結果もあります。特に前立腺がんを予防する効果は大規模な疫学研究で証明されています。
例えば、米国における47,882名の男性の食事の解析では、1週間に3回以上魚を食べるグループは、月に2回以下のグループと比較して、前立腺がんの発生頻度は7%の低下、進行した前立腺がんは17%の低下、転移のリスクは44%の低下を認めています。
スウェーデン人の6272名の男性を30年以上にわたって追跡調査した研究では、魚をほとんど食べないグループの前立腺がんの発生頻度は、魚を良く食べるグループの2~3倍でした。
DHAががん細胞の増殖速度を遅くしたり転移を抑制し、腫瘍血管新生を阻害し、がん細胞に細胞死(アポトーシス)を引き起こすことなどが多くのがん細胞で示されています。PGE2は血管新生を促進するので、PGE2産生を阻害するDHAには腫瘍血管の新生を阻害するようです。
その他にも、抗がん剤の効果を増強し副作用を軽減する効果や、がん性悪液質を改善する効果なども報告されています。がん性悪液質とは、がん細胞や炎症細胞から産生される炎症性サイトカイン(TNF-αやIL-6など)によって体重減少や食欲不振などの症状が出る状態です。DHAやEPAには、TNF-αやIL-6などの炎症性サイトカインの産生を抑える抗炎症作用があります。
免疫状態を改善し、感染症の予防効果も指摘されています。手術前や手術後にEPAやDHAを1日2〜3グラム補充した食事は、手術後の炎症を軽減し、体重減少や栄養状態の悪化を防ぐ効果があるという臨床試験の結果が多数報告されています。
手術侵襲によって挫滅した組織で炎症反応がおこり、炎症性サイトカインの産生などが原因となって筋肉や体重の減少が起こりますが、EPAやDHAは炎症性サイトカインの産生を抑えるなどの作用によって筋肉の異化を抑制し、体重減少を予防し術後の経過を良くします。
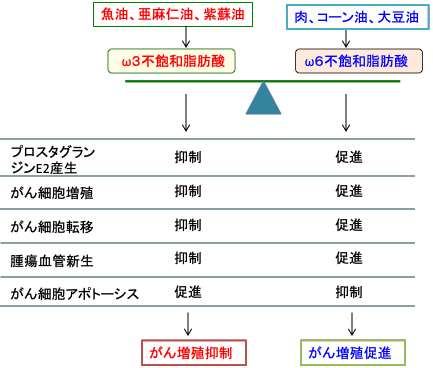
このようにDHAやEPAやαリノレン酸のようなω3系脂肪酸はがんの発育を抑制し、アラキドン酸のようなω6系脂肪酸はがんの発育を促進するので、摂取するω3系脂肪酸とω6系脂肪酸の比が腫瘍の発育に影響することになります。(下図)。
図:魚油・亜麻仁油・紫蘇油に多く含まれるω3系不飽和脂肪酸はがん細胞の増殖を抑制し、肉や食用油に含まれるω6系不飽和脂肪酸はがん細胞の増殖を促進する。ω6系不飽和脂肪酸の摂取量を減らしω3系不飽和脂肪酸を増やすとがん細胞の増殖を抑えることができる。
【多価不飽和脂肪酸は脂質二重層の流動性を高める】
脂肪は、それを構成している脂肪酸の構造の違いによって融点などの化学的性状が異なってきます。二重結合をもつ不飽和脂肪酸の多い脂肪は常温で液状になりますが、飽和脂肪酸になると固まりやすくなります。固まりやすい脂肪を多く摂取すると血液がドロドロになって動脈硬化が起こりやすくなります。
前述のように細胞膜は流動性を持ち、脂質や膜タンパク質は動いています。この流動性は膜の構成物質で決まります。特にリン脂質を構成する脂肪酸の不飽和度(二重結合の数)に影響されます。不飽和度が高まるほど脂肪酸の融点は低くなるためです。つまり、不飽和脂肪酸を多く含む細胞膜は流動性が高まります。脂肪酸は、構造の違いにより「飽和脂肪酸」と「不飽和脂肪酸」の2種類に分類できます。パルミチン酸(炭素数16)やステアリン酸(炭素数18)のように炭素と炭素の間に二重結合が全くない脂肪酸を飽和脂肪酸といい、二重結合がある脂肪酸を不飽和脂肪酸といいます。
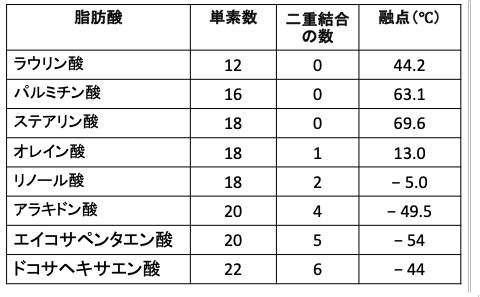
不飽和脂肪酸のうち炭素の二重結合が一つのものを「一価不飽和脂肪酸」、2つ以上あるものを「多価不飽和脂肪酸」といいます。一般に、脂肪酸は炭素の数が多くなるほど融点(固体から液体に変化する温度)が高くなります。また、同じ炭素数の脂肪酸を比較した場合、二重結合の数が多くなるほど融点が低くなります。(下表)
表:脂肪酸は炭素の数が多くなるほど融点(固体から液体に変化する温度)が高くなる。同じ炭素数の脂肪酸を比較した場合、二重結合の数が多くなるほど融点が低くなる。
原子は、他の原子と結合できる手を持ち、その数は原子毎に異なっています。炭素原子は、他の原子と結合できる手を4本持っています。炭素-炭素二重結合とは、2つの炭素原子どうしが互いに2本の手でつながっている状態のことをいい、「C=C」で表記します。
分子が接近すると分子間に引力のような力が働きます。この分子間引力をファンデルワールス力(van der Waals force)といいます。ファンデルワールス力は、分子間の距離が近づくほど強くなります。
飽和脂肪酸は炭素原子が直鎖状に並びます。まっすぐな棒状の構造なので、たくさんの分子が集まると、鉛筆を束ねた構造になります。したがって、ぎゅぎゅう詰めになるので、分子が動きにくくなり固体となります。ファンデルワールス力が強く働いて分子間の結合が強固になるためです。液体にするには熱を加え加えなければなりません。したがって、融点が高くなります。
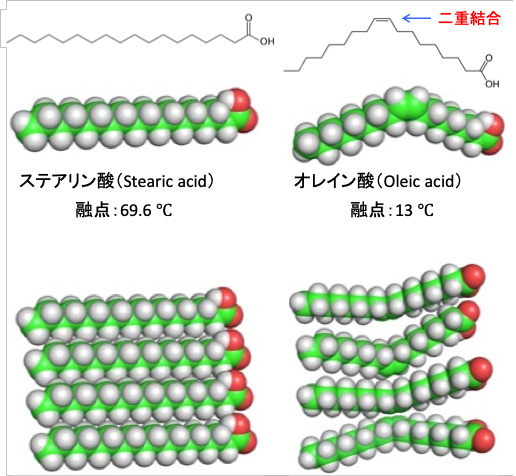
不飽和脂肪酸は二重結合の部分でくの字に曲がった構造になります。分子が曲がっているため、分子を束ねると隙間の多い構造になり、分子間のファンデルワールス力は弱くなります。その結果、分子は動き回ることができ、融点が低下して液体になります。(図)
図:脂肪酸のステアリン酸とオレイン酸は、どちらも18個の炭素原子で構成される。 ステアリン酸は炭素結合が全て飽和しているが、オレイン酸は不飽和脂肪酸であり、1つのシス二重結合を含んでいる。ファンデルワールス力いよる分子間の引力による結合はステアリン酸の方がオレイン酸よりはるかに強くなる。その結果、ステアリン酸の融点は69.9 ℃であり、オレイン酸の13℃の融点よりも高くなっている。不飽和脂肪酸が豊富な細胞膜は、飽和脂肪酸が豊富な膜よりも流動性が高くなる。
植物油や魚油が液体なのは不飽和脂肪酸が多いためです。細胞膜に不飽和脂肪酸が多く含まれるほど、流動性が高くなります。
体内の隅々の組織に酸素を運ぶ赤血球は、赤血球自身の直径よりも細い毛細血管を通過できます。赤血球の細胞膜が柔軟で、変形する能力をもっているためで、これを赤血球変形能といいます。赤血球の細胞膜の飽和脂肪酸の割合が大きくなると細胞膜の流動性が低下し、赤血球変形能が低下し、体の隅々まで酸素が行き渡らなくなります。食事からの不飽和脂肪酸の摂取が多いと、組織の血液循環が良くなります。
【人間の脳は魚を食べて大きくなった】
人類はオランウータンやゴリラやチンパンジーと共通の祖先から進化しました。動物進化の系統樹において、約1300万年前にオランウータン、約650万年前にゴリラ、約490万年前にチンパンジーが人類から分岐したと考えられています。人類の特徴は他の動物と比べて知能が高いことですが、知能の発達には脳が大きくなることが必須です。
チンパンジーの脳容積は400cc程度で、現代人の成人男性の脳容積の平均は約1350ccです。チンパンジーと同程度の脳容積しかなかった初期人類から、高度の知能をもった現生人類に進化する過程で脳容積は3倍以上に増えました。チンパンジーの脳容積は500万年前と同じで、人類の脳容積が3倍も増えた理由は、人類が動物性食糧を多く摂取するようになったからです。
脳組織の50から60%は脂質から構成されていますが、このうち約3分の1はアラキドン酸やドコサヘキサエン酸のような多価不飽和脂肪酸です。アラキドン酸は必須脂肪酸で人間は体内で合成できません。ドコサヘキサン酸は同じω3系不飽和脂肪酸のα-リノレン酸から体内で変換されることになっていますが、その効率は極めて悪いので、最近ではドコサヘキサエン酸も必須脂肪酸に分類されています。
つまり、脳の成長に必要なアラキドン酸とドコサヘキサエン酸は食事から摂取しなければなりませんが、この2つの脂肪酸は植物性食物には少ししか含まれていません。アラキドン酸は肉、ドコサヘキサエン酸は魚の脂に多く含まれています。
オランウータンやゴリラやチンパンジーのような類人猿から初期人類(猿人)にいたる1000万年以上の年月において、私たちの祖先はアフリカの森林に生息し、主に植物性の食物を食べていました。
約440万年前に現在のエチオピアの地域のジャングル(密林)に生息していた初期人類のラミドゥス猿人の食事は、木の葉や果実やベリー類など軟らかい植物性食物が主体でした。歯の構造から硬い植物を食べるようには適応していなかったようです。
約400万年〜200万年前に生存したアウストラロピテクスは二足歩行を行うようになり、密林からより開けた草原で住むようになります。アフリカ東部や南部のサバンナ(乾期と雨期のある熱帯に分布する疎林と灌木を交えた熱帯長草草原地帯)の環境に適応し、歯が発達して硬い殻をもつ大きな種子や地下の根なども食べるようになります。植物性食物を中心にして、さらに小動物の狩猟や、動物の死肉や肉食獣の食べ残しから動物質性食糧を得るようになりました。このような食生活が250万年くらい前から起こった気候の変化で変わっていきます。
人類が狩猟を開始する直接のきっかけは250万年前くらいから起こってきた気候や環境の変化です。このころから氷河期に移行し、地球上の気温が低下していき、アフリカのジャングルは縮小し、草原やサバンナに変化していったからです。
氷期の間は地球全体が乾燥し、降雨量が少なくなると大きな樹木は育たなくなり、草原が増えてきます。そこに草食動物が増え、草食動物を獲物とする大型の肉食動物が棲息するようになります。人類はそのような獣を狩猟によって食糧にしてきました。動物以外にも、漁によって魚介類も多く摂取しています。間氷期になって気候が暖かくなって樹木が成長すると木の実や果物なども増えますが、基本的には肉や魚など動物性の食糧が半分以上を占めていたようです。氷河期というのは地球の気候が長期にわたって寒冷化する期間で、北アメリカやヨーロッパ大陸に氷床が拡大し、アジアやアフリカも気温が低下して涼しくなり、熱帯性の密林は縮小していきます。氷河期は数万年続いて再び温かい気候に戻ります。氷期と氷期の間を間氷期と呼びます。
約250万年以降、4万年から10万年の周期で氷期と間氷期を繰り返しています。最後の氷期が終わったのが約1万年前で現在は間氷期にあたります。ホモ属(Homo)が現れたのは今から250万年〜200万年前です。ホモ属は現代の人類(ホモ・サピエンス)と同じ属です。この頃から人類は石器を道具として利用し、狩猟や肉食獣の食べ残しから得た動物性の食糧が増えてきます。さらに、160万年前くらいから人類は火を使うようになり、食物を火で加熱することによって栄養の吸収が良くなります。150万年前に住んでいたホモ・エレクトスは積極的に狩猟を行っていました。
このように初期人類の食事は植物性食糧由来の糖質が多いものでしたが、250万年くらい前から動物性食糧が増えるようになり、少なくとも150万年前くらいから農耕が始まる1万年前くらいまでは、低糖質・高蛋白食であったことになります。このような食事が人類を進化させました。
約1万年前に最後の氷河期が終わって地球が温暖化して農耕と牧畜が始まります。農耕によって穀物の摂取が増えました。糖質の摂取量は現代人では1日250から400グラム程度ですが、狩猟採集時代の糖質摂取量は1日10から125グラムと推定されています。
農耕が始まってから、成人の平均身長は減少しているという報告があります。また、骨粗しょう症や虫歯も増えています。そして、農耕が始まって人類の歴史の中ではじめて脳の重量が減少していることが報告されています。現代人の脳容積は、2万数千年前までヨーロッパに存在したネアンデルタール人の脳容積より10%程度小さいことが明らかになっています。その理由としてタンパク質や不飽和脂肪酸の摂取量の減少が指摘されています。農耕によって穀物が豊富になり、糖質が増えた分、肉や脂肪の摂取量が減ったからです。
魚油はオメガ3系不飽和脂肪酸のDHAとEPAが多いのですが、これは魚がDHAやEPAを合成しているわけではありません。DHAとEPAは微細藻類から由来します。つまり、ある種の微細藻類がDHAやEPAを合成し、それをプランクトンが食べ、プランクトンを小型魚が食べ、小型の魚が大型の魚(マグロ、カツオなど)に食べられるという食物連鎖によって大型魚にDHAとEPAが多く含まれることになります。それを人間が食べています。
温度が低下する海の中では、飽和脂肪酸が多い細胞膜は流動性が低下します。低温の環境でも細胞膜の流動性を維持するために藻類が高度多価不飽和脂肪酸を合成しているのかもしれません。人類はオメガ3系多価不飽和脂肪酸を多く摂取することによって脳が発達し、高度な知能を獲得しました。発育期の子供にDHA/EPAの摂取を増やすと頭が良くなるというデータは多く報告されています。子供の知能を高めたければ、脂ののった魚を多く食べさせるか、DHA/EPAのサプリメントを摂取することは有効です。高齢者の認知機能低下の予防にも有効です。
【ω3系不飽和脂肪酸を増やす食生活】
食事中の不飽和脂肪酸のオメガ6:オメガ3比は、狩猟採取で食品を確保していた旧石器時代の人類の食事では1〜2程度でしたが、近代における西洋型食事ではオメガ6:オメガ3比は20程度まで上昇しています。さらに動物性の飽和脂肪酸の摂取量も増えています。このような食事中の脂肪酸の組成の変化が、がんや心臓病、メタボリック症候群、炎症性疾患、自己免疫疾患の発症を促進していると考えられています。
アメリカ人の食事はω6:ω3の比が10~20になると報告されています。一方、伝統的な日本食(大豆と魚の豊富な食事)ではその比は1~2.8にあると言われています。しかし、日本でも食事の欧米化によってω6:ω3の比が高くなっています。
ω6:3の比を減らすとがんの発生や増殖や転移を減らすことができることが、大腸がん、乳がん、前立腺がんなどで確かめられています。
ω6:ω3の比を1~2以下にする食生活は、進行がんの食事療法として試してみる価値があります。肉類は極力控え、野菜はバランス良く摂取し、ω3不飽和脂肪酸の多い青背の魚(いわし・あじ・さば・さんま・まぐろなど)を食べます。野菜にはリノール酸などのω6脂肪酸が多いので、ω3不飽和脂肪酸のα-リノレン酸の豊富なシソ油か亜麻仁油をドレッシングとして使用するのが有効です。DHAやEPAは高熱で酸化しやすいので、魚は揚げ物や焼き魚は避け、生(刺身)か煮付けで食べることが大切です。
さらに、DHA/EPAのサプリメントを1日2~4グラム摂取すれば、ω6とω3の比をかなり下げることができます。免疫力が低下して生の食品摂取が危険な場合や魚が苦手な人もDHAやEPAのサプリメントを利用します。極端にω3脂肪酸を多くとると、血液が固まりにくくなるという副作用が出ますが、DHA/EPAのサプリメントを1日2~4グラム程度で、食事の内容を変えてω3不飽和脂肪酸を増やすのであれば、問題はありません。