2012年8月アーカイブ
ジインドリルメタンは卵巣がんに対するシスプラチンの抗腫瘍効果を増強する。
ジインドリルメタンは卵巣がんに対するシスプラチンの抗腫瘍効果を増強する。
ジインドルルメタンは転写因子のSTAT3(signal transducer and activator of
transcription 3)に作用して、マウスの動物実験モデルで卵巣がんの増殖を抑制し、シスプラチンの抗腫瘍効果を増強する。BMC Med. 2012 Jan 26;10:9.
【要旨】
研究の背景:Signal transducer and activator of
transcription 3 (STAT3:シグナル伝達兼転写活性化因子3)は卵巣がんの多くにおいて活性化されており、卵巣がんのシスプラチンに対する抵抗性獲得に関与している。
我々は、以前の研究において、ジインドリルメタンが卵巣がん細胞の増殖を阻害することを報告している。しかし、ジインドリルメタンの増殖抑制作用の作用機序については明らかにされていない。本研究では、ジインドリルメタンの作用機序を検討した。
実験方法:ヒト卵巣がん細胞株6種類を用いた培養細胞の実験系と、マウスに卵巣がん細胞を移植した動物実験モデルを用い、ジインドリルメタン単独の効果とシスプラチンとの併用効果について検討した。
結果:ジインドリルメタンは培養細胞の実験系で、6種類のヒト卵巣がん細胞全てに対してアポトーシス(細胞死)を誘導した。STAT3のTyr-705(チロシン705)とSer-727(セリン727)におけるリン酸化は、ジインドリルメタンによって用量依存的に抑制された。
さらに、ジインドリルメタンはSTAT3の核内への移行とDNA結合と転写活性を阻害した。インターロイキン-6によって誘導されるTyr-705におけるSTAT3のリン酸化もジインドリルメタンによって顕著に阻害された。
遺伝子導入によってSTAT3を過剰発現させると、ジインドリルメタンによって誘導されるアポトーシスは阻止された。さらに、卵巣がん細胞および卵巣がん組織におけるインターロイキン-6の発現量はジインドリルメタンによって減少した。
ジインドリルメタンは低酸素誘導性因子1α(HIF-1α)と血管内皮細胞増殖因子の発現を抑制してがん細胞の浸潤と血管新生を阻害した。
さらに重要なことは、ヒト卵巣がん細胞SKOV-3細胞におけるシスプラチンの作用をSTAT3を介する機序で増強した。
1日に3mgのジインドリルメタンの経口投与とシスプラチンの投与は移植腫瘍の増殖を著明に抑制した。腫瘍組織におけるアポトーシスの増加と、STAT3活性の抑制が認められた。
結論:以上の実験結果より、ジインドリルメタン単独あるいは抗がん剤との併用の有用性について卵巣がんの臨床例を対象に検討する価値がある。
【訳者注】
STAT3は、STAT (Signal Tranducer and Activator of Transcription:シグナル伝達兼転写活性化因子) ファミリーに属する蛋白質で、その名の通り、シグナル伝達と遺伝子転写活性化の両方において働きます。STAT3は非活性化状態においては細胞質に存在しますが、Janusキナーゼ(JAK)が活性化されることによってリン酸化を受け、核内へ移行して目的遺伝子を活性化する転写因子として機能します。
IL-6ファミリーのサイトカインあるいはEGF等の成長因子がそれらの受容体に結合することによりJanusキナーゼ(JAK)が活性化されると、活性化されたJAKがSTAT3のチロシン705をリン酸化します。
チロシン705がリン酸化されたSTAT3二分子のSH2ドメインがそれぞれ他方の分子のリン酸化チロシンと相互作用することにより二量体を形成して核内に移行し、核内に移行したSTAT3二量体は標的となるDNAに結合する事で転写を活性化します。これをJAK-STAT経路と言います。STAT3は種々の腫瘍に恒常的に発現しておりますが、STAT3の機能を阻害するとアポトーシスが誘導されることから、STAT3阻害剤は新たな抗がん剤のターゲットとして着目されています。
この論文では、ジインドリルメタンは卵巣がんに対するシスプラチンの効果を増強し、その機序としてSTAT3の活性化を抑制する効果を示唆しています。
ジインドリルメタンに関しては、Akt/NF-κBシグナル伝達系を阻害する作用によって、がん細胞の細胞死(アポトーシス)を誘導する作用や抗がん剤に対する感受性(抗がん剤が効きやすくなること)を高める効果が報告されています。
例えば、乳がん細胞に対するタキソールの効果、前立腺がん細胞の対するタキソテールの効果、膵臓がんに対する抗がん剤(シスプラチン、ジェムシタビン、オキサリプラチン)やタルセバ(erlotinib)の効果を高めることが報告されています。
さらに、NF-κBの活性を阻害することによって、NF-κBによって調節を受け、血管新生やがん細胞の浸潤や転移に関与しているVEGFやIL-8やMMP-9やuPAなどの遺伝子発現を抑え、がん細胞の増殖や転移を抑える効果も報告されています。
様々な機序によって抗がん剤感受性を高める効果が報告されていますので、ジインドリルメタンは抗がん剤治療と併用するサプリメントとして極めて有用だと言えます。
ジインドリルメタンのサプリメントについてはこちらへ;
原文:
BMC Med. 2012 Jan 26;10:9.
Diindolylmethane suppresses ovarian
cancer growth and potentiates the effect of cisplatin in tumor mouse model by
targeting signal transducer and activator of transcription 3 (STAT3).
Source
Department of Biomedical Sciences
and Cancer Biology Center, Texas Tech University Health Sciences Center,
Amarillo, TX 79106, USA.
Abstract
BACKGROUND:
Signal transducer and activator of
transcription 3 (STAT3) is activated in majority of ovarian tumors and confers
resistance to cisplatin treatment in patients with ovarian cancer. We have
reported previously that diindolylmethane (DIM) inhibits the growth of ovarian
cancer cells. However, to date the exact mechanism by which DIM induces growth
suppressive effects has not been clear. In this report the mode of action of
DIM is investigated.
METHODS:
Six human ovarian cancer cell lines
and an ovarian tumor xenograft animal model were used to study the effect of
diindolylmethane alone or in combination with cisplatin.
RESULTS:
Diindolylmethane treatment induced
apoptosis in all six ovarian cancer cell lines. Phosphorylation of STAT3 at
Tyr-705 and Ser-727 was reduced by DIM in a concentration-dependent manner. In
addition, diindolylmethane treatment inhibited nuclear translocation, DNA
binding, and transcriptional activity of STAT3. Interleukin (IL)-6-induced
phosphorylation of STAT3 at Tyr-705 was significantly blocked by DIM.
Overexpression of STAT3 by gene transfection blocked DIM-induced apoptosis. In
addition, DIM treatment reduced the levels of IL-6 in ovarian cancer cells and
in the tumors. DIM treatment also inhibited cell invasion and angiogenesis by
suppressing hypoxia-inducible factor 1α (HIF-1α) and vascular epithelial growth
factor (VEGF). Importantly, diindolylmethane treatment potentiated the effects
of cisplatin in SKOV-3 cells by targeting STAT3. Oral administration of 3 mg
diindolylmethane per day and subsequent administration of cisplatin
substantially inhibited in vivo tumor growth. Western blotting analysis of
tumor lysates indicated increased apoptosis and reduced STAT3 activation.
CONCLUSIONS:
These findings provide a rationale
for further clinical investigation of DIM alone or in combination for
chemoprevention and/or chemotherapy of ovarian cancer.
牛蒡子(ゴボウシ)に含まれるアルクチゲニンは小胞体ストレスを軽減する。
牛蒡子(ゴボウシ)に含まれるアルクチゲニンは小胞体ストレスを軽減する。
アルクチゲニンはAMPKを活性化することによって小胞体ストレスを軽減する。(Acta Pharmacol Sin. 33(7):941-52, 2012)
【要旨】
目的:生薬の牛蒡子(ゴボウシ)に含まれるリグナン(phenylpropanoid
dibenzylbutyrolactone lignan)の一種のアルクチゲニン(Arctigenin)の、小胞体ストレスに対する保護作用とそのメカニズムをin
vitro(試験管内)の実験系で検討した。
方法:小胞体ストレスを調節する物質を探索するための培養細胞を用いたスクリーニング系を確立した。細胞生存率はMTTアッセイ法で測定し、遺伝子や蛋白質の発現はPCRやウェスタンブロット法で検討した。CaMKKβ, LKB1, AMPKα1遺伝子の抑制(サイレンシング)はRNA干渉法で行った。
細胞内のATP量はATPバイオルミネッセント•アッセイキットを用いて測定した。
結果:小胞体ストレスを誘導するbrefeldin A(100 nmol/L)の添加によって培養細胞に引き起こされた細胞死と小胞体ストレス応答を、アルクチゲニン((2.5, 5 and 10 μmol/L)は用量依存的に阻害した。
アルクチゲニン(1, 5 and 10 μmol/L)はmTOR-p70S6Kシグナル伝達系とeEF2(eukaryotic translation elongation
factor 2)活性を阻害することによって蛋白合成を顕著に抑制し、この抑制作用はRNA干渉法でAMPKの発現を抑制すると部分的に阻止された。アルクチゲニン(1-50 μmol/L)はミトコンドリアの電子伝達系の呼吸鎖複合体-Iを阻害することによってATPの細胞内レベルを低下させ、AMPKを活性化した。
AMPK阻害剤のCompound C (25 μmol/L)で細胞を前処理すると、小胞体ストレスに対するアルクチゲニンの抑制作用は阻止された。さらに、アルクチゲニン(2.5 and 5 μmol/L)はAMPKを活性化し、2mmol/Lのパルミチン酸塩(palmitate)でINS-1 β細胞に誘導した小胞体ストレスと細胞死を抑制した。
結論:アルクチゲニンはAMPKを活性化し、蛋白質合成を抑制し、小胞体への負荷を軽減することによって、小胞体ストレスから細胞を守る効果がある。
【訳者注】
AMPKはAMP活性化プロテインキナーゼ(AMP-activated protein kinase)の略です。AMPKは人から酵母まで真核細胞に高度に保存されているセリン・スレオニンキナーゼ(セリン・スレオニンリン酸化酵素)の一種で、代謝物感知タンパク質キナーゼファミリー(metabolite-sensing protein kinase family)のメンバーとして細胞内のエネルギーのセンサーとして重要な役割を担っています。
全ての真核生物は、細胞が活動するエネルギーとしてアデノシン三リン酸(Adenosine Triphosphate:ATP)というヌクレオチドを利用しています。ATPは「生体のエネルギー通貨」と言われ、エネルギーを要する生物体の反応過程には必ず使用されています。ATPがエネルギーとして使用されるとADP(Adenosine Diphosphate:アデノシン-2-リン酸)とAMP(Adenosine Monophosphate:アデノシン-1-リン酸)が増えます。すなわち、ATP → ADP + リン酸 → AMP+2リン酸というふうに分解され、リン酸を放出する過程でエネルギーが産生されます。AMPKはこのAMPで活性化されるタンパクリン酸化酵素で、低グルコース、低酸素、虚血、熱ショックのような細胞内 ATP 供給が枯渇する状況において、AMPの増加に反応して活性化されます。
AMPKは細胞内エネルギー(ATP)減少を感知して活性化し、異化の亢進(ATP産生の促進)と同化の抑制(ATP消費の抑制)を誘導し、ATPのレベルを回復させる効果があります。すなわち、AMPKが活性化すると、糖や脂肪や蛋白質の合成は抑制され、一方、糖や脂肪や蛋白質の分解(異化)が亢進してATPが産生されます。
がん細胞ではAMPKの活性が抑制されており、AMPKを活性化するとがん細胞の増殖を抑制できることが報告され、AMPKはがんの予防や治療のターゲットとして有望視されています。AMPKの活性化ががん細胞の増殖を抑制する効果があることは、培養がん細胞や移植腫瘍を使った動物実験など多くの基礎研究で明らかになっています。
mTORはmammalian target of rapamycin(哺乳類ラパマイシン標的タンパク質)の略です。
mTORはラパマイシン(放線菌の一種から見つかった物質で免疫抑制作用や抗がん作用を持つ)の標的分子として同定されたセリン・スレオニンキナーゼで、細胞の分裂や生存などの調節に中心的な役割を果たすと考えられています。がん細胞ではmTORの活性が亢進しており、mTORの活性を阻害すると、がん細胞の増殖や血管新生を阻害することができます。mTOR阻害剤ががんの治療薬として臨床ですでに使用されています。AMPKはmTOR経路を阻害して蛋白質の合成を抑制し、がん細胞の増殖や血管新生を阻害します。
小胞体ストレス(Endoplasmic reticulum stress)とは、正常な高次構造に折り畳まれなかったタンパク質(変性タンパク質:unfold protein)が小胞体に蓄積し、それにより細胞への悪影響、つまりストレスが生じることです。
細胞内のリボソームで合成された蛋白質は、小胞体で修飾を受け、高次構造(折り畳み)を形成しながら成熟蛋白質となって細胞外へ搬出されます。正常な折り畳みがなされた蛋白質はゴルジ体へ送られますが、折り畳みに失敗した異常な蛋白質は小胞体にとどまります。このような正常な高次構造に折り畳まれなかった異常蛋白質が小胞体内に蓄積して、細胞への悪影響(=ストレス)が生じることを小胞体ストレス(ERストレス:Endoplasmic
reticulum stress)と言います。
小胞体ストレスは細胞の機能を妨げるため、細胞にはその障害を回避する仕組みが備わっています。この小胞体ストレスに対する細胞反応を小胞体ストレス応答 (unfold protein response: UPR) といいます。
小胞体ストレスの原因となる変性タンパク質は、遺伝子変異、ウイルス感染、炎症、有害化学物質、栄養飢餓、低酸素(虚血)などにより生じます。変性タンパク質は小胞体ストレスセンサー(IRE1alpha, ATF6, Perk など)によって感知され、小胞体ストレス応答を誘導します。小胞体ストレス応答は、蛋白質の産生量を低下させることで小胞体におけるタンパク質の折りたたみ負荷を軽減したり、分子シャペロンの量を増やすことで折りたたみ機能を向上させたり、変性タンパク質の除去効率をあげることで小胞体ストレスを取り除くよう働きます。
変性タンパク質が過剰に蓄積し、小胞体ストレスの強さが細胞の回避機能を越えると、細胞死(アポトーシス)が誘導されます。小胞体ストレスはアルツハイマー病などの神経変性疾患などさまざまな疾患の原因となると考えられています。
この論文は、細胞に引き起こされた小胞体ストレスを牛蒡子に含まれるアルクチゲニン(Arctigenin)が軽減し、小胞体ストレスから細胞を守るという内容です。そのメカニズムとして、アルクチゲニンはAMPKを活性化し、mTORシグナル伝達を抑制し、蛋白質合成を抑制して小胞体への負荷を軽減することによって小胞体ストレスを軽減するということです。
小胞体ストレスは糖尿病やパーキンソン病や動脈硬化性疾患など様々な疾患の発症と深く関連していることが知られています。したがって、小胞体ストレスを軽減する効果はこれらの疾患の予防や治療に役立つ可能性があります。また、AMPKの活性化やmTOR阻害作用はがん治療にも役立つ可能性を示唆しています。
牛蒡子(ゴボウシ)はキク科のゴボウArctium lappa L. の果実(種子)です。牛蒡(ゴボウ)の根は食用に供されますが、種子は牛蒡子という生薬名で薬用に用いられます。
牛蒡子には解毒、解熱、消炎、排膿の作用があり、咽の痛い風邪、扁桃腺炎、化膿性の腫れ物、湿疹、麻疹、歯茎の腫れなどに応用されています。牛蒡子の配合される漢方処方には柴胡清肝湯(さいこせいかんとう)、消風散(しょうふうさん)、銀翹散(ぎんぎょうさん)などがありますが、これらは風邪や湿疹や慢性炎症やアトピー体質の治療に使われます。
牛蒡子には抗炎症作用や抗菌作用、抗腫瘍作用が報告されており、清熱解毒薬に分類されます。牛蒡子の抗炎症作用や抗腫瘍作用は、それに含まれるアルクチイン(arctiin)やアルクチゲニン(arctigenin)などのリグナン誘導体によるものと考えられています。
この論文から、牛蒡子は小胞体ストレスを軽減することで、様々な変性性疾患にも効果があることが示唆されます。
図:リボソームで作られた蛋白質は、小胞体で修飾を受けて高次構造(折り畳み)を形成し、さらにゴルジ体で糖鎖の結合などによって成熟蛋白質となって細胞外へ搬出、あるいは細胞内で利用される。低酸素やグルコース枯渇や栄養飢餓状態が起こると、折り畳みに異常をきたした不良蛋白質が小胞体に蓄積する。これを『小胞体ストレス』という。牛蒡子に含まれるアルクチゲニンは、AMP活性化プロテインキナーゼを活性化し、mTORシグナル伝達系を阻害し、蛋白合成を抑制して小胞体の負荷を減らし、小胞体ストレスを軽減する作用が報告されている。
原文:
Acta Pharmacol Sin. 2012 Jul;33(7):941-52. doi: 10.1038/aps.2012.60.
Epub 2012 Jun 18.
Arctigenin
alleviates ER stress via activating AMPK.
Gu Y, Sun XX, Ye JM, He L, Yan SS, Zhang HH, Hu LH, Yuan JY, Yu Q.
Source
Department of Tumor
Pharmacology, Shanghai Institute of Materia Medica, Chinese Academy of
Sciences, Shanghai 201203, China.
Abstract
Aim:To investigate the protective effects of arctigenin (ATG), a phenylpropanoid dibenzylbutyrolactone lignan from Arctium lappa L (Compositae), against ER stress in vitro and the underlying mechanisms.Methods:A cell-based screening assay for ER stress regulators was established. Cell viability was measured using MTT assay. PCR and Western blotting were used to analyze gene and protein expression. Silencing of the CaMKKβ, LKB1, and AMPKα1 genes was achieved by RNA interference (RNAi). An ATP bioluminescent assay kit was employed to measure the intracellular ATP levels.Results:ATG (2.5, 5 and 10 μmol/L) inhibited cell death and unfolded protein response (UPR) in a concentration-dependent manner in cells treated with the ER stress inducer brefeldin A (100 nmol/L). ATG (1, 5 and 10 μmol/L) significantly attenuated protein synthesis in cells through inhibiting mTOR-p70S6K signaling and eEF2 activity, which were partially reversed by silencing AMPKα1 with RNAi. ATG (1-50 μmol/L) reduced intracellular ATP level and activated AMPK through inhibiting complex I-mediated respiration. Pretreatment of cells with the AMPK inhibitor compound C (25 μmol/L) rescued the inhibitory effects of ATG on ER stress. Furthermore, ATG (2.5 and 5 μmol/L) efficiently activated AMPK and reduced the ER stress and cell death induced by palmitate (2 mmol/L) in INS-1 β cells.Conclusion:ATG is an effective ER stress alleviator, which protects cells against ER stress through activating AMPK, thus attenuating protein translation and reducing ER load.
ケトン食は悪性グリオーマの放射線治療の補助療法として有効
ケトン食は悪性グリオーマの放射線治療の補助療法として有効
PLoS
One. 2012;7(5):e36197. Epub 2012 May 1.
【要旨】
ケトン食は高脂肪、低炭水化物(低糖質)の食事で、血中のケトン体の濃度を高めることによって体内のエネルギー代謝を変える。KetoCal® は市販されている食品で、ケトン比(脂肪:炭水化物+蛋白質)が4:1で必須栄養素を完全に含んでおり、難治性のてんかんのに対する非薬物治療として有効性が認められている。この食事によって誘導されるケトン血症は脳細胞の恒常性に変化を与え、悪性グリオーマなど他の神経疾患の治療にも効果が期待されている。
我々は、悪性グリオーマの頭蓋内生体蛍光マウスモデル( intracranial bioluminescent mouse model of malignant glioma)を用い、グリオーマ細胞を移植後、標準的な食事を与えるグループとケトン食を与えるグループに分けた。それぞれのグループに2x4Gの全脳照射を行い、腫瘍の増殖を生体内イメージングによって追跡した。
ケトン食を与えたマウスではケトン体のβヒドロキシ酪酸の血中濃度を上昇し、平均生存期間は標準食を与えられたマウスより約5日間延長した。
ケトン食と放射線治療の併用療法は相和効果以上であり、ケトン食を与えられて照射を受けた11匹のマウスのうち9匹において、腫瘍細胞からの生体蛍光シグナルは検出限界以下まで消滅した。ケトン食のマウスは腫瘍移植後101日後に標準食に変更したが、200日以上に渡って再発を認めなかった。
結論として、ケトン食は放射線治療の抗腫瘍効果を著明に増強した。この結果は、ケトン食によって誘導される細胞内代謝の変化は、ヒトの悪性グリオーマの標準的治療の補助療法として有用であることが示唆された。
【訳者注】
脳腫瘍に対して、ケトン食はそれだけで延命効果があり、放射線治療と併用すると、相和(additive)以上の効果で、顕著な腫瘍縮小効果を示したという内容です。ケトン食によってケトン体(アセト酢酸やβヒドロキシ酪酸)が増加し、これらケトン体はがん細胞のエネルギー産生を阻害し、放射線感受性を高めるという作用機序のようです。
脳腫瘍に対してケトン食が有効であるという報告は多数あります。この論文もその一つで、ケトン体が脳腫瘍の放射線感受性を高めるという結果を報告しています。脳腫瘍の放射線治療の最中にケトン食を実践することは有効だと言えます。
Abstractの原文
PLoS One. 2012;7(5):e36197. Epub 2012 May 1.
The ketogenic
diet is an effective adjuvant to radiation therapy for the treatment of
malignant glioma.
Abdelwahab MG, Fenton KE, Preul MC, Rho JM, Lynch A, Stafford P, Scheck AC.
Source
Neuro-Oncology Research, Barrow
Neurological Institute® of St. Joseph's Hospital and Medical Center, Phoenix,
Arizona, United States of America.
Abstract
INTRODUCTION:
The ketogenic diet (KD)
is a high-fat, low-carbohydrate diet that alters metabolism by increasing
the level of ketone bodies in the blood. KetoCal® (KC) is a nutritionally
complete, commercially available 4:1
(fat:carbohydrate+protein) ketogenic formula that is an effective
non-pharmacologic treatment for the management of refractory pediatric
epilepsy. Diet-induced ketosis causes changes to brain homeostasis that
have potential for the treatment of other neurological diseases such as
malignant gliomas.
METHODS:
We used an intracranial
bioluminescent mouse model of malignant glioma. Following implantation
animals were maintained on standarddiet (SD) or KC. The mice received 2×4
Gy of whole brain radiation and tumor growth was followed by in vivo imaging.
RESULTS:
Animals fed KC had elevated
levels of β-hydroxybutyrate (p = 0.0173) and an increased median survival of
approximately 5 days relative to animals maintained on SD. KC plus radiation
treatment were more than additive, and in 9 of 11 irradiated animals maintained
on KC the bioluminescent signal from the tumor cells diminished below the level
of detection (p<0.0001). Animals were switched to SD 101 days after
implantation and no signs of tumor recurrence were seen for over 200 days.
CONCLUSIONS:
KC significantly enhances the
anti-tumor effect of radiation. This suggests that cellular metabolic
alterations induced through KC may be useful as an adjuvant to the current
standard of care for the treatment of human malignant gliomas.
マンゴスチンにがん抑制効果・・・岐阜大教授ら立証
マンゴスチンにがん抑制効果・・・岐阜大教授ら立証
(2012年5月28日読売新聞)
東南アジア原産の果物「マンゴスチン」の果皮に含まれるポリフェノールの一種「キサントン」に、がん抑制効果があることを、岐阜薬科大学の飯沼宗和教授(生薬学)と岐阜大学大学院の赤尾幸博教授(腫瘍(しゅよう)医学)が動物実験などで立証し、がんの補完代替医療に役立つ健康食品として実用化した。
マンゴスチンの厚い果皮は、東南アジア地域では古くから伝承薬として用いられ、抗菌や抗カビ作用があることで知られる。両教授は、果皮の主成分キサントンを抽出し、培養したヒトのがん細胞と大腸ポリープを発症したラットを使い、その効果を確かめる実験を行った。
その結果、ヒトのがん細胞は、キサントンを低濃度で加えると48時間後に6〜7割が死滅。ラットでは、0.05%の非常に薄い濃度でエサに混ぜて食べさせると、食べない場合と比べてポリープの数が約半数に減ることが分かった。いずれも副作用はなかった。
両教授は、キサントンの成分だけを抽出する方法も開発し、特許を取得。県や企業、病院などと連携し、キサントンの研究会を発足させ、がん治療を補完する健康食品(錠剤)として、現在、薬局や医療機関での普及を図っている。
赤尾教授は「キサントンには抗酸化や免疫活性化の作用もあり、がん予防や再発を抑えるなどの機能性食品として優れている」と話している。
キサントンのサプリメントについてはこちらへ
ハーブ系サプリメントのBreastDefendはトリプルネガティブの乳がんの転移を抑制する
ハーブ系サプリメントのBreastDefendはトリプルネガティブの乳がんの転移を抑制する
タイトル(日本語訳):
BreastDefendはトリプルネガティブのヒト乳がんの正所性移植腫瘍動物モデルにおいて肺への転移を予防する Oncol Rep 2012 July 26. doi: 10.3892/or.2012.1936. [Epub ahead of print]
【要旨】
BreastDefendはキノコのカワラタケ (Coriolus
versicolor)、 霊芝(Ganoderma
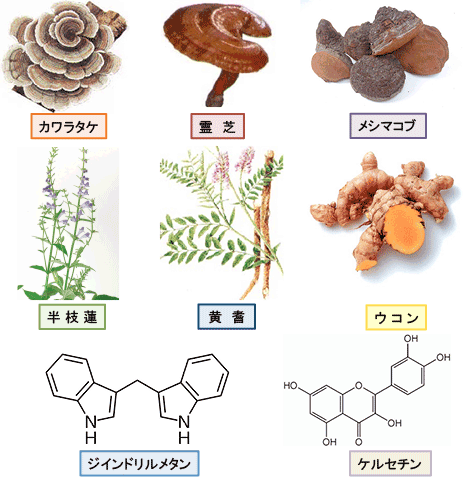
lucidum)、 メシマコブ(Phellinus linteus)、 生薬の半枝蓮(Scutellaria barbata)、黄耆( Astragalus membranaceus)、ウコン(Curcuma longa)の抽出エキスと食品由来生理活性成分のジインドリルメタンとケルセチン を加えたサプリメントである。このBreastDefendがヒト浸潤性乳がん細胞由来のMDA-MB-231の増殖と転移を阻害することをin vitro(試験管内)の実験で示している。
今回の研究は、マウスに移植した乳がん細胞の増殖と肺への転移に対してBreastDefendが抑制効果を示すかどうかを検討するために行った。
マウスに体重1kg当たり100mgのBreastDefendを4週間経口投与したが、体重や肝機能は変化がなく、組織学的にも肝臓や脾臓や肺や心臓の組織に毒性は認められなかった。
さらに、コントロール群に比べて、BreastDefend投与群では移植腫瘍の著明な縮小を認めた。肺への転移は、コントロール群(BreastDefend非投与)では67%に見られたのに対して、BreastDefend投与群では20%に顕著に低下した。転移数の中央値はコントロール群が2.8(最小0.0、最大48.0)に対してBreastDefend投与群では0.0(最小0.0、最大14.2)であった。BreastDefendの転移抑制効果は、転移関連遺伝子のPLAU(ウロキナーゼ・プラスミノーゲン・アクチベーター)とCXCR4(C-X-Cケモカイン受容体-4)の乳がん組織における発現低下によって確認された。
結論として、BreastDefendは浸潤性乳がんの治療手段と有望であることが示唆された。
【訳者注】
乳がんに対して抗がん作用を示すハーブや薬草や食品成分に関しては多くの報告があります。BreastDefendは米国のサプリメントの商品名ですが、Breastは「乳房」Defendは「守る」という意味で乳腺の健康を守るような効果を期待させる商品名です。この中には、キノコのカワラタケ、レイシ、メシマコブ、抗がん生薬として多くの報告があり乳がんに対する有効性が報告されている半枝蓮、免疫力を高める黄耆(オウギ)、抗炎症作用やがん予防効果が報告されているウコン、アブラナ科野菜に含まれる成分で乳がんの予防効果があるジインドルルメタン、がん予防効果があるフラボノイドの一種のケルセチンと、乳がんの予防や治療に効果が期待できそうな成分を組み合わせた組成になっています。
このような組合せは、漢方薬やサプリメントを使った乳がんの治療でもポピュラーな組合せです。動物実験のレベルですが、乳がんの増殖や転移を抑制する効果が示されていますので、乳がんに対する漢方治療やサプリメントの有効性を示唆する根拠になると思います。この製品は米国で販売されていますが、サプリメントで摂取するよりも、漢方薬の煎じ薬にジインドリルメタンのサプリメントを併用する方が効果が高いと思います。
乳がんの漢方治療についてはこちらへ:
ジインドリルメタンについてはこちらへ:
原文:
Oncol Rep. 2012 Jul 26. doi: 10.3892/or.2012.1936. [Epub ahead of print]
BreastDefend™
prevents breast-to-lung cancer metastases in an orthotopic animal model of
triple-negative human breast cancer.
Jiang J, Thyagarajan-Sahu
A, Loganathan J,
Eliaz I,
Terry C,
Sandusky GE,
Sliva D.
Source
Cancer
Research Laboratory, Methodist Research Institute, Indiana University Health,
Indianapolis, IN 46202, USA.
Abstract
メラトニンは卵巣がんに対するシスプラチンのアポトーシス誘導効果を増強する
メラトニンは卵巣がんに対するシスプラチンのアポトーシス誘導効果を増強する
タイトル(日本語訳):
『メラトニンは卵巣がん細胞SK-OV-3細胞において、ERK/p90 リボゾームS6キナーゼ/ヒートショック蛋白27の脱リン酸化を介して、シスプラチンによって誘導されるアポトーシスを相乗的に促進する』J Pineal Res. 2012 Mar;52(2):244-52.
【要旨】
シスプラチンによる卵巣がんに対する治療の効果を、メラトニンが高めるかどうかを検討するために、この実験は行われた。
ヒト卵巣がん細胞のSK-OV-3細胞に対してメラトニンは単独では細胞毒性を示さないが、シスプラチンは用量依存的に細胞生存率を抑制する。
シスプラチンとメラトニンを併用すると、SK-OV-3細胞の生存率を相乗的に減少させた。
一方、正常な卵巣細胞であるOSEN細胞に対しては、メラトニンはシスプラチンの細胞毒性からOSEN細胞を保護する作用を示した。
シスプラチン単独で投与した場合に比べて、シスプラチン+メラトニンを投与した場合は、がん細胞(SK-OV-3細胞)のsub-G1期のDNA量と、TdT-mediated dUTP nick end-labeling (TUNEL)-陽性細胞が増加した。これは、シスプラチンによる卵巣がん細胞のアポトーシス誘導をメラトニンが増強することを意味している。シスプラチンとメラトニンの併用投与はcaspase-3とpoly-(ADP-ribose) polymerase (PARP)の切断を増やした。
重要なことは、メラトニンはシスプラチンによって誘導される 90-kDa
ribosomal S6 kinase (p90RSK) とヒートショックタンパク( heat shock protein)27 (HSP27) を脱リン酸化させ、同時にextracellular signal-regulated kinase (ERK)のリン酸化を相乗的に阻害した。
さらに、シスプラチン投与によって誘導されるp90RSK とHSP27の発現と共存在(colocalizaton)をメラトニンは著明に阻害した。
これらの結果より、ヒト卵巣がん細胞SK-OV-3細胞のERK/p90RSK/HSP27 cascadeの不活性化を介して、メラトニンはシスプラチンによるアポトーシスを促進することが示された。
【訳者注】
シスプラチンを投与すると、がん細胞はシスプラチンに抵抗しようと細胞内シグナル伝達系を活性化してアポトーシスを起こしにくくするメカニズムが作用します。この耐性獲得にextracellular signal-regulated kinase (ERK)/90-kDa ribosomal S6 kinase (p90RSK) /ヒートショックタンパク( heat shock protein)27 (HSP27) のリン酸化が関与しており、メラトニンはこのリン酸化を阻害することによって、卵巣がん細胞に対するシスプラチンのアポトーシス誘導作用を増強するという結果です。
培養細胞を使ったin vitro(試験管内)の実験なので、生体内でどの程度効果があるかは不明ですが、卵巣がんのシスプラチン治療に対してメラトニンを併用する根拠になるかもしれません。
メラトニンについてはこちらへ
英文原文:
J Pineal Res. 2012
Mar;52(2):244-52.
Melatonin
synergistically enhances cisplatin-induced apoptosis via the dephosphorylation
of ERK/p90 ribosomal S6 kinase/heat shock protein 27 in SK-OV-3 cells.
Kim JH, Jeong SJ, Kim B, Yun SM, Choi do Y, Kim SH.
Source
College of Oriental
Medicine, Kyung Hee University, Seoul, South Korea.
Abstract
To evaluate melatonin's ability to enhance ovarian cancer cells to cisplatin treatment for ovarian cancer, this study was performed. Melatonin by itself had no significant cytotoxicity against SK-OV-3 cells, while cisplatin suppressed the cell viability in a dose-dependent manner. Combined treatment with cisplatin and melatonin synergistically inhibited the viability of SK-OV-3 cells with the synergism between two drugs (1 > combination index). In contrast, melatonin revealed the protective effect against cisplatin-induced cytotoxicity in OSEN normal ovarian epithelial cells. Cotreatment with cisplatin and melatonin increased the sub-G1 DNA contents and TdT-mediated dUTP nick end-labeling (TUNEL)-positive cells compared with cisplatin control in SK-OV-3 cells, suggesting that melatonin augments cisplatin-induced apoptosis. Consistently, combined treatment of cisplatin and melatonin increased the cleavage of caspase-3 and poly-(ADP-ribose) polymerase (PARP). Importantly, melatonin synergistically inhibited the phosphorylation of extracellular signal-regulated kinase (ERK) along with dephosphorylation of 90-kDa ribosomal S6 kinase (p90RSK) and heat shock protein 27 (HSP27) induced by cisplatin. Furthermore, melatonin remarkably blocked the expression and colocalization of p90RSK and HSP27 by combination treatment with cisplatin. Taken together, our findings demonstrate that melatonin enhances cisplatin-induced apoptosis via the inactivation of ERK/p90RSK/HSP27 cascade in SK-OV-3 cells as a potent synergist to cisplatin treatment.